|
||||
|
|
27. Свойства серной кислоты и ее практическое значение Структура формулы серной кислоты: 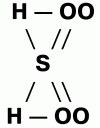 Получение: основным методом производства серной кислоты из SO3 является контактный метод. Вначале получают диоксид серы SO2 (сжигание серы и др.). Самый распространенный способ получения – обжиг серного колчедана FeS2, затем диоксид серы SO2 окисляют в триоксид серы SO3 контактным методом. Полученный три-оксид серы SO3 направляют на стадию поглощения, которую проводят концентрированной серной кислотой. Раствор SO3 в H2SO4 называется олеум. Контактным методом получают 92,5 %-ную серную кислоту. При нитрозном методе H2SO4 получают, окисляя SO2 в сернокислотном растворе, для этого в качестве катализатора используют смесь оксидов азота NO и NO2. Нитрозным методом получают 75 %-ную серную кислоту. Чтобы приготовить раствор серной кислоты, ее необходимо выливать в воду тонкой струйкой, сильно перемешивая, при этом в воде образуются гидраты и происходит выделение теплоты. Физические свойства: Серная кислота – бесцветная вязкая жидкость, имеющая температуру плавления 10 °C, температура кипения 296 °C (с разложением на H2O и SO3). Серная кислота – сильная кислота. Концентрированная серная кислота в большом количестве поглощает пары воды, поэтому ее используют для осушения газов. Химические свойства. 1. Концентрированная серная кислота является сильным окислителем. Окислительно-восстановительные реакции требуют нагревания, а продуктом реакции в основном является SO2. 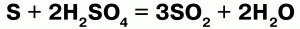 2. С металлами вступает в реакцию по-разному в зависимости от концентрации. Разбавленная серная кислота взаимодействует со всеми металлами, стоящими в ряду напряжений до водорода. Концентрированная серная кислота окисляет все металлы, стоящие в ряду напряжений, и серебро в том числе. 3. Разбавленная серная кислота взаимодействует с основаниями, основными и амфотерными оксидами, солями. Серная кислота образует два вида солей: средние (сульфаты) и кислые (гидросульфаты). Применение: серная кислота относится к главным продуктам химической промышленности. Ее используют для изготовления фосфорных и азотных удобрений, искусственных волокон, моющих средств, взрывчатых веществ, лекарственных препаратов. С ее помощью получают другие кислоты, сульфаты, очищают нефтепродукты, применяют как электролит в свинцовых аккумуляторах, подготавливают поверхность металлов для гальванических покрытий. |
|
||
|
Главная | В избранное | Наш E-MAIL | Прислать материал | Нашёл ошибку | Наверх |
||||
|
|
||||
